INTRODUCCIÓN
La trombosis es una de las principales causas de morbilidad y mortalidad en todo el mundo y representa un importante problema de salud pública. El tromboembolismo venoso (TEV), que incluye la trombosis venosa profunda y la embolia pulmonar, se considera el tercer trastorno cardiovascular más común después de la enfermedad de las arterias coronarias y el accidente cerebrovascular. Su etiología es multifactorial y resulta de la interacción entre factores genéticos y adquiridos que alteran el equilibrio del sistema hemostático.
Estas condiciones pueden clasificarse como trombofilias hereditarias, asociadas con variantes genéticas que afectan proteínas involucradas en la hemostasia, y trombofilias adquiridas, relacionadas con factores clínicos como cirugía, embarazo, inmovilización prolongada, uso de anticonceptivos hormonales o enfermedades inflamatorias [2,3].
Entre las variantes genéticas más estudiadas en relación con el riesgo de trombosis se encuentran el Factor V Leiden (G1691A), la protorombina G20210A y la variante C677T del gen de la metilenetetrahidrofolato reductasa (MTHFR). El Factor V Leiden es una de las trombofilias hereditarias más comunes y se ha asociado con un mayor riesgo de tromboembolismo venoso.
Del mismo modo, la variante G20210A de la protorombina ha estado vinculada a un aumento del riesgo trombótico. La variante C677T del MTHFR, asociada con hiperhomocisteinemia, ha sido ampliamente estudiada en pacientes con eventos trombóticos y pérdidas recurrentes de embarazo; sin embargo, su asociación directa con la trombosis venosa sigue siendo controvertida en la literatura científica.
Durante el embarazo, se desarrolla un estado fisiológico de hipercoagulabilidad, lo que aumenta el riesgo trombótico. Este fenómeno también se ha relacionado con complicaciones obstétricas como la pérdida recurrente de embarazo (RPL), definida como la pérdida de dos o más embarazos consecutivos antes de las 20 semanas de gestación (American College of Obstetricians and Gynecologists [ACOG]) [6]. Aunque la etiología de la RPL es multifactorial, se han investigado las trombofilias hereditarias como posibles factores contribuyentes en un subgrupo de pacientes.
En América Latina, y particularmente en Panamá, la información sobre la prevalencia de variantes genéticas asociadas con la trombofilia es limitada. Por lo tanto, este estudio tuvo como objetivo determinar la prevalencia de las variantes Factor V Leiden (G1691A), protrombina G20210A y MTHFR C677T en pacientes con eventos tromboembólicos y pérdida recurrente del embarazo, así como en controles sanos de una población panameña.
MATERIALES Y MÉTODOS
Diseño del estudio
Se llevó a cabo un estudio observacional, analítico y de casos y controles basado en la población para determinar la prevalencia de las variantes genéticas Factor V Leiden (G1691A), prolamina G20210A y MTHFR C677T en una población panameña.
Población de estudio
La población del estudio consistió en pacientes evaluados en el Laboratorio de Genética del Complejo Hospitalario Dr. Arnulfo Arias Madrid, Panamá.
Se incluyeron dos grupos de estudio:
Grupo A (pérdida recurrente del embarazo): Se incluyeron cincuenta y cinco mujeres panameñas con antecedentes de dos o más pérdidas recurrentes del embarazo, que fueron referidas para pruebas de trombofilia genética desde enero de 2013. El grupo de control consistió en 55 mujeres sin antecedentes de pérdida recurrente del embarazo o trombosis y con al menos un embarazo a término.
Grupo B (eventos tromboembólicos)
Se incluyeron ciento cinco pacientes con antecedentes de eventos tromboembólicos, referidos por los departamentos de Diagnóstico Prenatal, Hematología, Ginecología-Obstetricia y Neurología. Estos pacientes habían experimentado accidente cerebrovascular, trombosis venosa profunda o tromboembolismo pulmonar sin otros factores de riesgo asociados. El grupo de control correspondiente estaba formado por 105 individuos panameños sin antecedentes de trombosis.
Las edades de los participantes variaron de 18 a 44 años en el grupo de RPL y de 20 a 70 años en el grupo de eventos tromboembólicos.
Se excluyeron a los pacientes con inmunosupresión primaria o adquirida, procesos infecciosos agudos, cáncer o cualquier condición que impidiera la comprensión del estudio, ya sea debido a enfermedades neurológicas o psiquiátricas o barreras idiomáticas.
Recolección de muestras y extracción de ADN
Se utilizó sangre periférica recolectada en tubos de anticoagulante EDTA para la extracción de ADN. El ADN genómico se extrajo de 200 μL de sangre utilizando el kit QIAamp DNA Mini Blood y el sistema automatizado QIAcube (QIAGEN), siguiendo las instrucciones del fabricante [7].
Detección de variantes genéticas
La identificación de las variantes Factor V Leiden (G1691A), prothrombin G20210A y MTHFR C677T se realizó mediante PCR multiplex en punto final utilizando el kit de trombofilia Elucigene TRP (Gen-Probe). El método se basa en el enfoque ARMS-PCR (Sistema de Mutación Réfractor de Amplificación) [8], que permite la detección de mutaciones puntuales a través de la amplificación específica de alelos [9], siguiendo las instrucciones del fabricante. Cada reacción incluyó controles de amplificación internos. Los productos amplificados se separaron por electroforesis en un gel de agarosa al 2% y se visualizaron bajo luz ultravioleta para determinar el genotipo correspondiente.
Análisis estadístico
Se calcularon las frecuencias genotípicas y alélicas de las variantes estudiadas. Las variables continuas, como la edad, se describieron utilizando la media y el rango. La asociación entre las variantes genéticas y los eventos trombóticos o la pérdida recurrente del embarazo se evaluó utilizando tablas de contingencia 2×2 y el cálculo de razones de momios (OR) con intervalos de confianza del 95% (IC del 95%) [10].
RESULTADOS
Un total de 320 individuos fueron analizados, distribuidos en dos grupos de estudio y sus controles correspondientes. El Grupo A incluyó a 55 mujeres con pérdida recurrente del embarazo (RPL), de 18 a 44 años (edad media: 32 años), y 55 controles con al menos un embarazo a término y sin historial de RPL o trombosis. El Grupo B consistió en 105 pacientes con eventos tromboembólicos (TEE), de 20 a 67 años (edad media: 37 años), de los cuales el 90% eran mujeres y el 10% eran hombres. El grupo de control correspondiente incluyó a 105 individuos sanos, de 20 a 75 años (edad media: 42 años), de los cuales el 84% eran mujeres y el 16% eran hombres.
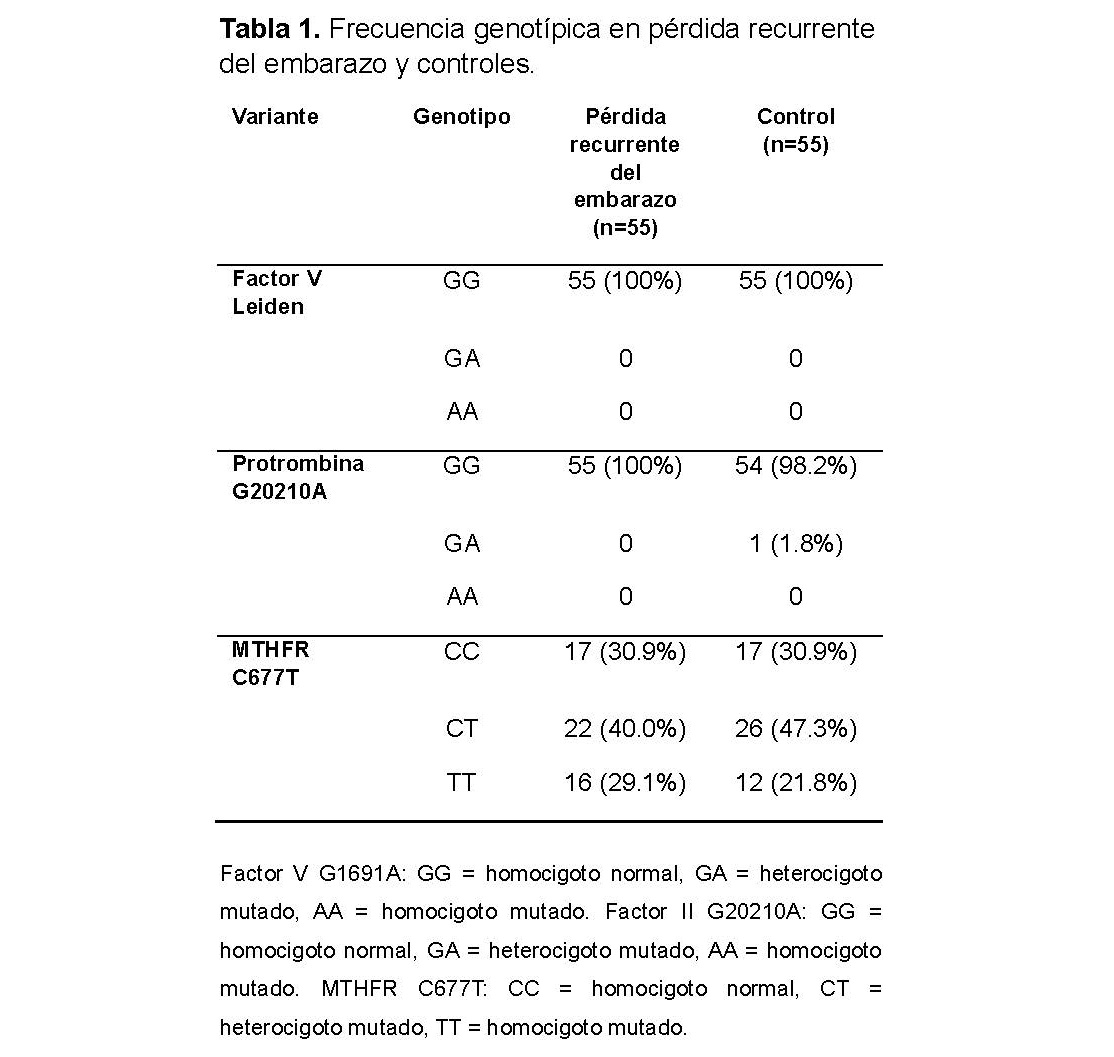
El factor V Leiden (G1691A) y las variantes de protrombina G20210A no fueron detectados en pacientes con pérdida recurrente del embarazo (Tabla 1). Solo se identificó un individuo heterocigoto para la protrombina G20210A en el grupo de control, lo que corresponde a una prevalencia del 0.9%. Con respecto a la variante MTHFR C677T, se observaron 22 pacientes heterocigotos (40%) y 16 pacientes homocigotos (29.1%) en el grupo de RPL, mientras que se identificaron 26 controles heterocigotos (47.3%) y 12 controles homocigotos (21.8%) en el grupo de control. La prevalencia alélica fue del 49.1% en pacientes y del 45.5% en controles, sin evidencia de asociación con la pérdida recurrente del embarazo (OR = 1.0; 95% CI: 0.44–2.24).
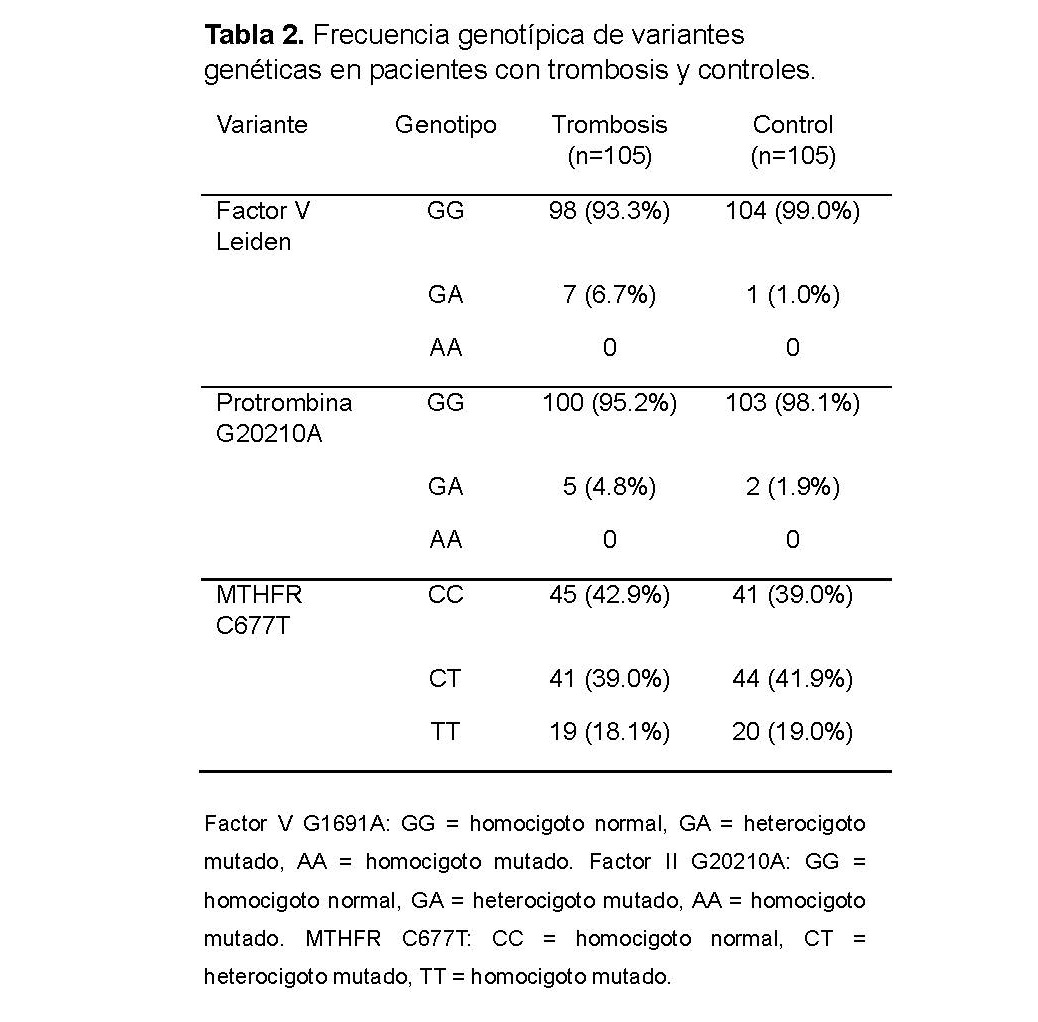
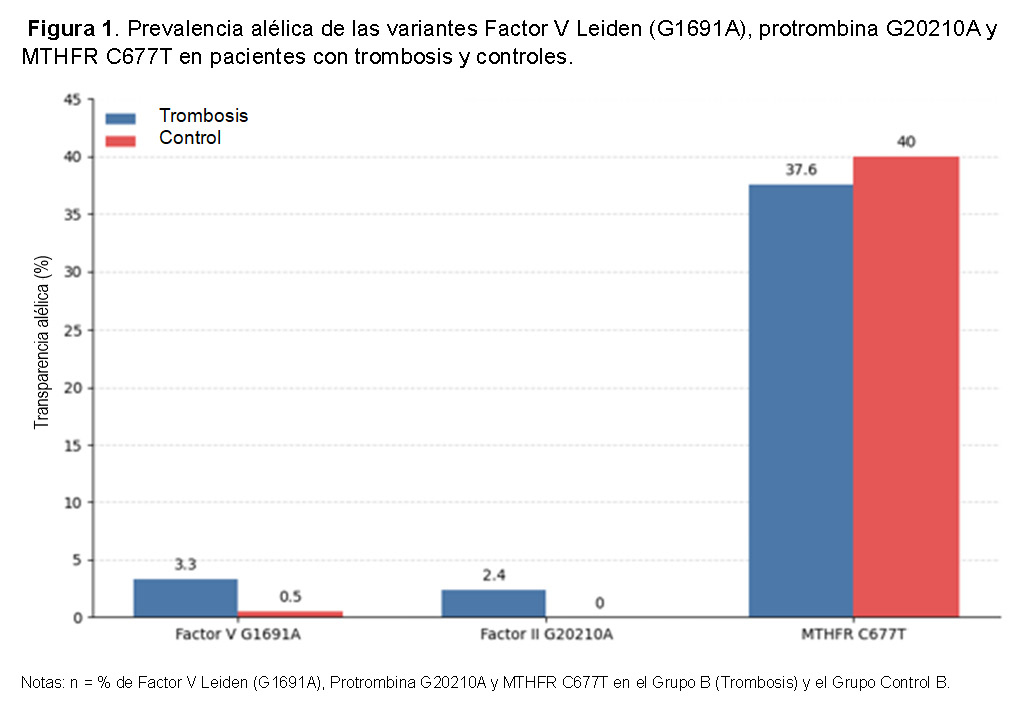
En el grupo de trombosis, se identificaron 7 individuos heterocigotos para el Factor V Leiden (6.7%) (Tabla 2), mientras que se detectó 1 individuo heterocigoto (1.0%) en el grupo de control, sin casos homocigotos. Esta variante mostró una asociación con un aumento del riesgo de trombosis (OR = 7.43; IC del 95%: 0.89–61.48). La variante de la protrombina G20210A se detectó en 5 pacientes con trombosis (4.8%) y 2 controles (1.9%), todos heterocigotos, con una asociación moderada con la trombosis (OR = 2.58; IC del 95%: 0.48–13.58). En cuanto a la variante MTHFR C677T, se observaron 41 pacientes heterocigotos (39.0%) y 19 pacientes homocigotos (18.1%) en el grupo de trombosis, mientras que se identificaron 44 controles heterocigotos (41.9%) y 20 controles homocigotos (19.0%) en el grupo de control. La prevalencia alélica fue del 37.6% en pacientes y del 40.0% en controles, sin evidencia de asociación con eventos tromboembólicos (OR = 0.85; IC del 95%: 0.49–1.48) (Figura 1).
DISCUSIÓN
Los resultados del presente estudio indican que la variante del Factor V Leiden (G1691A) está asociada con un aumento del riesgo de trombosis en la población analizada. Se observó una heterocigosidad del 6.7% en pacientes con eventos tromboembólicos, comparado con el 1.0% en los controles, lo que corresponde a un aumento aproximado del riesgo de trombosis de siete veces (OR = 7.43; 95% IC: 0.89–61.48). Este hallazgo es consistente con estudios previos que muestran un aumento significativo en el riesgo tromboembólico entre los portadores heterocigotos de esta variante, que conduce a resistencia a la proteína C activada y promueve un estado pro-trombótico [11].
Al comparar con los resultados reportados en otras poblaciones, se observan frecuencias de heterocigosidad variables, incluyendo el 2.6% en Argentina, 5.4% en Chile, 6% en Brasil y 8% en los Estados Unidos, mientras que se han reportado prevalencias del 28% en Costa Rica y del 14.3% en Nicaragua en América Central [12,13,14,15,16,17]. Estas diferencias reflejan la heterogeneidad genética entre poblaciones; sin embargo, la frecuencia observada en la población panameña se encuentra dentro del rango reportado en la región.
En cuanto a la variante G20210A de la protrombina, se observó una prevalencia del 2.4% en pacientes con trombosis y del 1.0% en controles, con frecuencias heterocigotas del 4.8% y 1.9%, respectivamente, lo que sugiere una asociación moderada con el riesgo trombótico (OR = 2.58; 95% CI: 0.48–13.58), inferior a la observada para el Factor V Leiden. La frecuencia encontrada es comparable a la reportada en Chile (5.4%), Estados Unidos (5.0%) y Argentina (5.1%), y ligeramente superior a la reportada en Brasil (3.0%) [13,15,12,14].
La relación entre las trombofilias hereditarias y la pérdida recurrente de embarazo (PRA) sigue siendo controvertida. Aunque algunos estudios han sugerido una posible asociación, la evidencia disponible es heterogénea y el cribado rutinario en mujeres sin antecedentes obstétricos adversos no se recomienda ampliamente. En concordancia con este contexto, no se detectaron variantes del Factor V Leiden y de la protrombina G20210A en el grupo de PRA analizado en este estudio, y por lo tanto, no se observó ninguna asociación con esta condición. Este resultado es consistente con estudios realizados en poblaciones latinoamericanas, como un estudio de cohorte en Argentina que también no encontró diferencias significativas en la distribución de variantes trombofílicas entre pacientes con pérdida recurrente de embarazo y controles fértiles.
En cuanto a la variante MTHFR C677T, se observaron frecuencias similares entre pacientes y controles en ambos grupos, de trombosis y RPL, sugiriendo que esta variante no constituye un factor de riesgo independiente para estas condiciones en la población estudiada. Aunque puede estar asociada con niveles elevados de homocisteína, su impacto clínico como factor de riesgo trombótico es limitado, y su alta frecuencia en la población general puede explicar la ausencia de una asociación significativa [20,21].
En conjunto, estos hallazgos apoyan la noción de que las trombofilias hereditarias actúan principalmente como factores predisponentes, cuyo efecto clínico depende de la interacción con otros factores genéticos y ambientales.
CONCLUSIONES
Este estudio caracterizó la prevalencia del Factor V Leiden, prothrombin G20210A y la variante MTHFR C677T en pacientes panameños con eventos tromboembólicos y pérdida recurrente del embarazo (RPL). Se observó una fuerte asociación entre el Factor V Leiden y la trombosis, con un aumento de aproximadamente siete veces en el riesgo trombótico, mientras que prothrombin G20210A mostró una asociación moderada. No se encontró asociación entre estas variantes y RPL, ni entre la variante MTHFR C677T y eventos trombóticos o gestacionales. Estos hallazgos resaltan la importancia de las pruebas de trombofilia hereditaria en pacientes con trombosis para respaldar la toma de decisiones clínicas y la evaluación del riesgo familiar.
Limitaciones y recomendaciones
Se recomiendan estudios prospectivos para evaluar las concentraciones de ácido fólico y vitamina B12, ambos cofactores de la enzima MTHFR, en pacientes con el genotipo homocigoto, y correlacionarlas con los niveles plasmáticos de homocisteína, dado que la hiperhomocisteinemia se ha asociado con un aumento del riesgo trombótico. También sería relevante explorar la posible interacción genética entre el Factor V Leiden y la variante de MTHFR, así como su coexistencia con otras trombofilias hereditarias, con el fin de evaluar su efecto sinérgico sobre la predisposición a eventos trombóticos.
Agradecimientos
Al Laboratorio de Genética del Complejo Hospitalario Dr. Arnulfo Arias Madrid, Caja de Seguro Social, Panamá, por su apoyo en la realización de las determinaciones de laboratorio.
Contribuciones de los autores
JC: estandarización de pruebas, conceptualización, análisis de datos, redacción de manuscritos, revisión y escritura. OE: conceptualización de manuscritos. LDG: apoyo en la conceptualización y redacción de manuscritos. LS: revisión, corrección de protocolos y redacción de protocolos.
Conflicto de intereses / Divulgación
Todos los autores declaran que participaron en el diseño, ejecución y análisis del artículo y aprobaron la versión final. Además, no hay conflictos de interés relacionados con este artículo.
Disponibilidad de datos
Todos los datos que respaldan los hallazgos de este estudio están disponibles dentro del artículo. Información adicional está disponible del autor de correspondencia previa solicitud razonable.
